У людей с болезнью Паркинсона наблюдается потеря клеток мозга, продуцирующих дофамин, что приводит к тремору, ригидности, брадикинезии и постуральной нестабильности - основным симптомам заболевания.
Потеря продуцирующих дофамин нейронов является патологическим признаком болезни Паркинсона. Однако точные механизмы остаются неясными. Группа исследователей из Университета Сеченова и Университета Питтсбурга представила наиболее перспективные стратегии применения генной инженерии для изучения и лечения болезни Паркинсона.
Новый метод может помочь изучить роль клеточных процессов в прогрессировании заболевания, разработать перспективные методы лечения и лекарственные препараты, а также оценить их эффективность с использованием модельных организмов.
Болезнь Паркинсона (БП) - это нейродегенеративное заболевание, которое влияет на двигательную активность, включая равновесие и координацию. Во всем мире около 6,5 миллионов человек болеют болезнью Паркинсона в 2016 году по сравнению с 2,5 миллионами в 1990 году.
В Австралии распространенность БП была выше, чем многие виды рака в 2014 году, и, по оценкам, один из каждых 308 человек живет с болезнью Паркинсона.
Механизмы мозга запускают прогрессирование заболевания
Нейродегенеративное расстройство имеет много двигательных и когнитивных нарушений и обычно наблюдается у пожилых людей, которым более 55 лет. Болезнь прогрессирует медленно и постепенно, со временем ухудшая состояние. В тяжелых случаях пациент может испытывать трудности с движениями, разговором и самостоятельными действиями, такими как забота о себе.
Лечение необходимо для того, чтобы помочь улучшить качество жизни людей, страдающих от этой болезни. Опубликованное в журнале Free Radical Biology and Medicine исследование подчеркивает, как механизмы в мозге вызывают развитие и прогрессирование БП.
Ученые обнаружили большое количество механизмов, которые, вероятно запускают и ускоряют развитие болезни Паркинсона. Они выяснили, что в 10 % всех случаев существует генетическая предрасположенность к БП. В большинстве случаев заболевания были обусловлены как генетическими рисками, так и окружающей средой.
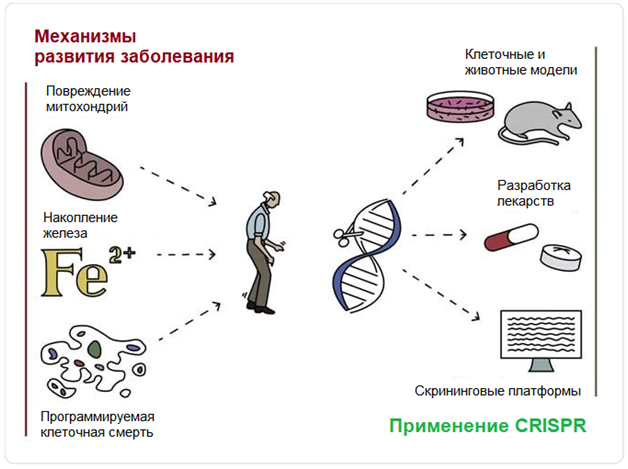
В то время как аберрантный окислительно-восстановительный метаболизм связан с дисрегуляцией обмена железа и повреждением митохондрий и рассматривается как один из основных факторов нейродегенерации и гибели дофаминергических клеток, конкретные механизмы развития заболевания до сих пор неясны.
Исследователи сосредоточили внимание на вероятных причинах заболевания, которые связаны с окислительно-восстановительными реакциями в клетках, и механизмами гибели клеток, называемыми апоптозом и ферроптозом.
CRISPR является многообещающим методом, который может помочь в разработке новых и эффективных методов лечения нейродегенеративных заболеваний. Существует большое количество способов, которыми CRISPR может помочь в лечении болезни Паркинсона.
Митохондрии и патогенез болезни Паркинсона
Первая группа механизмов связывает роль митохондрий с патологией болезни Паркинсона. Митохондрии, являются клеточными электростанциями, они образуют активные формы кислорода (АФК), которые важны для регуляции клеточного гомеостаза и передачи сигналов. Когда в митохондриях происходит повреждение, АФК накапливается и вызывает повреждение клеточных структур.
Поскольку повреждение митохондрий может привести к гибели всей клетки, важно, чтобы старые и поврежденные митохондрии были немедленно устранены в процессе, называемом митофагия. Но, когда наблюдается избыточная или неэффективная митофагия, возможно появление нейродегенерации.
У людей с мутацией в генах PINK1 и Parkin, которые кодируют белки, необходимые для функционирования митохондрий, наблюдалась мышечная дегенерация, митохондриальная дисфункция и потеря дофаминергических клеток мозга, что характерно для болезни Паркинсона.
В таком сценарии CRISPR может помочь в поиске неизвестных генов и их белковых продуктов, которые могут являться причинами развития и прогрессирования заболевания. Изучение этих белков может способствовать разработке новых лекарств и методов лечения людей с БП
Гомеостаз железа и функционирование клеток
Гомеостаз - это внутренний баланс процессов организма. Железо и АФК важны для правильного функционирования клеток, и, если есть какие-либо изменения в их обмене, это может привести к нарушению жизненно важных клеточных процессов.
Если существует дисбаланс в железе, оно может накапливаться в тканях мозга пожилых людей. Чаще всего они откладываются в тех участках мозга, которые контролируют двигательные и когнитивные функции. Как было установлено в предыдущих исследованиях, высокий уровень железа в черной субстанции сопровождался дофаминергической гибелью клеток головного мозга.
Технология CRISPR может помочь в разработке лекарств, которые могут нормализовать баланс железа в пораженных участках мозга.
Апоптоз и ферроптоз
Еще одна важная группа процессов – это механизмы программируемой клеточной гибели – апоптоз и ферроптоз. Белки и ДНК клеток расщепляются ферментами во время апоптоза. После чего происходит ферроптоз, при котором происходит железо-зависимое окисление липидов. Побочные продукты окисления накапливаются в клетке, что приводит к токсическим эффектам. Эти программы гибели клеток могут способствовать развитию нейродегенеративных заболеваний, поскольку они ускоряют гибель клеток, в том числе дофаминергических нейронов. CRISPR может помочь в этом случае, предоставив подробные исследования путей гибели клеток, что позволит лучше понять их роль в развитии болезни Паркинсона и других заболеваний головного мозга.
«Это один из многих важных шагов на пути к внедрению этой новой технологии для лечения пациентов с серьезными заболеваниями, такими как нейродегенеративные расстройства. Данный метод уже использовался в исследованиях на людях (в Китае, Германии, США) для лечения больных раком на поздней стадии и бета-талассемией», - поясняет автор исследования Маргарита Артюхова.
«Такие исследования позволяют нам рассматривать огромный потенциал редактирования генома как терапевтической стратегии. Трудно оставаться спокойным, когда вы понимаете, что прогресс технологий редактирования генома может полностью изменить наше понимание лечения болезни Паркинсона и других нейродегенеративных расстройств», - добавляет ученый.
Источник перевода: www.news-medical.net